La découverte de cibles potentielles (ou biomarqueurs) associées au phénomène biologique étudié est une étape cruciale dans la conception d'un traitement ou d'un test diagnostic.
Dans de nombreux cas c'est au niveau du protéome que se décide la différence entre la maladie et la bonne santé. Cette différence peut être suivie pour diagnostiquer les maladies ou essayer de rétablir une activité normale par des médicaments.
Nos approches se basent essentiellement sur des techniques de nano chromatographie haute performance couplée à la spectrométrie de masse haute résolution (LC-MS/MS) qui permettent de d'identifier et de quantifier plusieurs centaines de protéines simultanément.
Les matériels biologiques peuvent être des fluides tels que plasmas, sérums, urines, des prélèvements de tissus ou des cultures cellulaires.
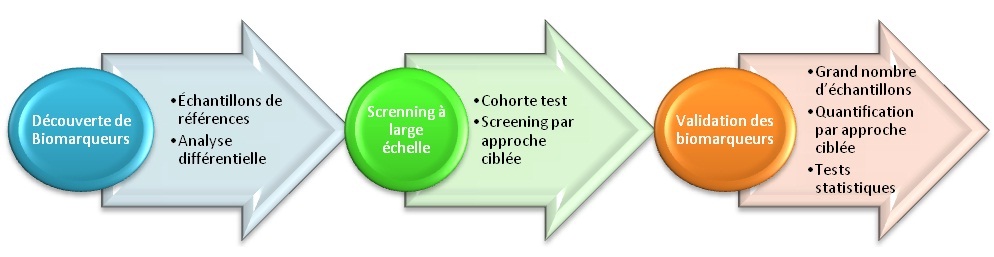
Il est recommandé d'effectuer l'analyse sur environ 6 échantillons de chaque condition testée, dans le but d'avoir des hypothèses statistiques solides.
Cette méthode permet de comparer entre eux des échantillons (e.g traité vs contrôle) à travers leur profil LC-MS mono ou bidimensionnelle et en identifiant les composés différenciants par MS/MS (full scan MS). Elle permet également d'avoir accès à la quantification relative et a pour avantage d'être soutenue par des tests statistiques puissants que sont l'analyse en composante principale couplée au test de Student. De plus, l'autre avantage de cette méthode est qu'elle ne nécessite pas d'étape marquage ou de dérivations complexes et coûteuses des échantillons.
Cette approche que nous utilisons le plus souvent est une approche type « label free » qui présente l'avantage d'être facile à appréhender et peu coûteuse. Cependant en fonction de la demande nous pouvons également réaliser des approches utilisant le marquage isobarique (TMT®) qui reste cependant une solution plus coûteuse.
La comparaison des protéines aux bases de données existantes permet l'identification des protéines différenciantes. Si elles ne sont pas connues, il est possible de les caractériser.
Le nombre d'échantillons cliniquement documentés pertinents est de plusieurs dizaines.
La prise en compte d'une protéine et des nombreux peptides qui en sont issus par la fragmentation dans la chaîne MS (Parallel Reaction Monitoring) permet d'obtenir une quantification absolue des protéines différenciantes.
Les méthodes ciblées type PRM sont considérées comme les plus sélectives et les plus sensibles des méthodes de spectrométrie de masse. En effet en utilisant le mode de scan MRM, les composés subissent une filtration sur le parent MS et les fragments MS/MS ce qui a pour effet d'augmenter la sensibilité de l'analyse et de sortir les composés d'intérêts du bruit de fond. L'utilisation d'un analyseur haute résolution (Orbitrap) couplé avec un analyseur effectuant une filtration ionique précise (Quadripôle) des parents permet d'obtenir des méthodes de quantification et de screening type PRM à haute résolution où le compromis sensibilité/spécificité est beaucoup plus favorable que sur un instrument type triple quadripôle en mode PRM classique. L'avantage de ce genre de technique ciblée est de pouvoir suivre les composés d'intérêts de manière robuste et rapide. De plus, les méthodes PRM haute résolution sont transposables sur des instruments de type triple quadripôle sous forme de méthode PRM.
Etude clinique complète comparativement à une technique de référence.